Miíase, conhecida popularmente como calcanhar de maracujá, é a infestação de vertebrados vivos com larvas dípterosas. Dependendo da localização do corpo e da relação das larvas com o hospedeiro, o parasita pode causar uma ampla gama de condições médicas. A miíase continua sendo um grande problema econômico na pecuária, pois leva à redução da produção de leite, problemas de peso e fertilidade, além de reduzir a qualidade da pele, com consequentes perdas econômicas. A miíase humana é encontrada em todo o mundo, mas com mais espécies e maior abundância em regiões socioeconômicas pobres de países tropicais e subtropicais. Em países não endêmicos, o calcanhar de maracujá também é uma condição importante, pois pode representar a quarta doença de pele associada à viagem mais comum.
A miíase é uma zoonose derivada do grego (mya, ou mosca) que cobre uma variedade de associações entre larvas dipterosas e mamíferos. É a infestação de humanos vivos ou animais vertebrados com larvas díspares que, pelo menos por um certo período, se alimentam do tecido morto ou vivo do hospedeiro, substância líquida do corpo ou alimento ingerido. A distribuição é mundial, com mais espécies e maior abundância em áreas tropicais, subtropicais e temperadas quentes. A doença de animais domésticos é um problema agrícola global. A infestação nosocomial raramente tem sido relatada. O histórico apropriado de viagem ou exposição em um ambiente clínico compatível deve alertar o clínico para a possibilidade de miíase.
As espécies mais comuns de moscas botânicas são a Dermatobia hominis e a Cochliomyia hominivorax do Novo Mundo. A doença mais comumente ocorre em áreas tropicais como México, América do Sul, América Central e Caribe. Os ovos são colocados no solo ou em pisos de areia. Quando as larvas eclodem à noite, elas procuram uma refeição de sangue de hospedeiros humanos adormecidos. A mordida pode ser ligeiramente dolorosa e pode causar edema local. A miíase cutânea é a mais comum, mas a miíase nasofaríngea tem sido relatada e descreve a infestação do nariz, boca, seios nasais e ouvido. O tratamento consiste na remoção das larvas de forma manual ou cirúrgica.
A miíase é frequentemente caracterizada clinicamente como uma função do local da infestação. Na maioria das vezes, as larvas ocorrem dentro da pele e podem se manifestar como furuncular, migratória, ou ferida ou miíase traumática. A forma mais comum de miíase humana é conhecida como miíase furuncular, na qual as larvas de mosca se encaixam na pele de uma pessoa. A lesão resultante assemelha-se a uma fervura ou furúnculo; é uma placa edematosa ou nódulo tenro, vermelho, de aproximadamente 1-3 cm de diâmetro, com uma fina abertura no ápice central da lesão. Essa abertura é um poro, através do qual a larva em desenvolvimento respira. A miíase furuncular na América Central e do Norte do Sul é mais frequentemente causada pela Oestridae, D. hominis, e lesões similares na África equatorial a C. antropophaga.
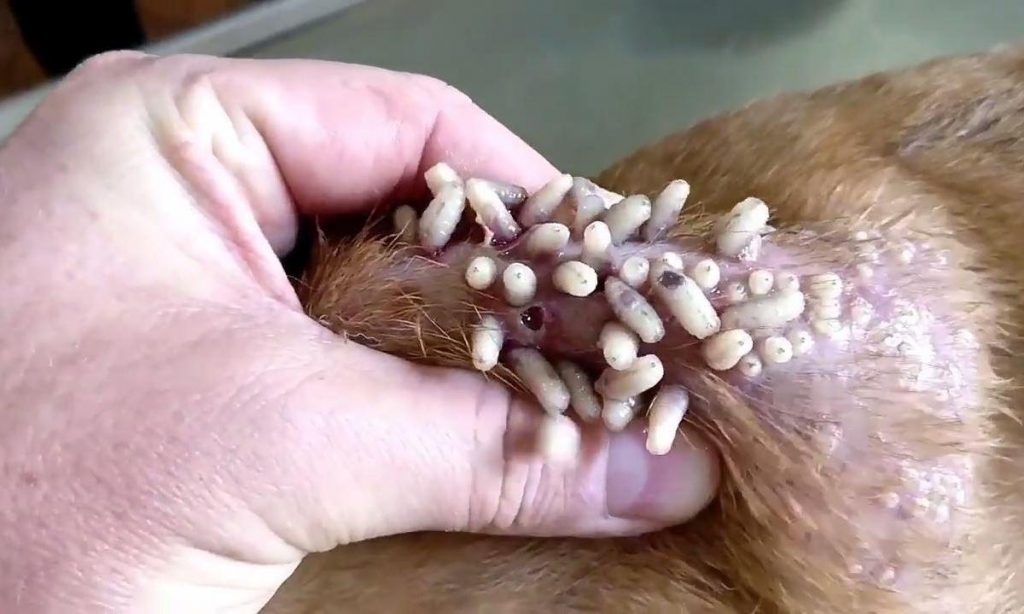
Feridas traumáticas, feridas supurativas, erosões abertas e úlceras e tecidos em decomposição expostos são particularmente atraentes para várias espécies de moscas que depositarão seus ovos diretamente dentro ou perto das margens da ferida. Larvas de outras moscas infestam cavidades e orifícios naturais em sítios nasofaríngeos, urogenitais e intestinais, ou invadem e se desenvolvem dentro do olho ou tecidos mais profundos. A miíase da ferida pode até se iniciar dentro de um ambiente hospitalar e se desenvolver sob curativos e curativos.
O calcanhar de maracujá tende a ser autolimitado, com poucos casos manifestando-se com mais do que patologia clínica mínima. Os movimentos de desenvolvimento das larvas, entretanto, podem resultar em inflamação e desconforto acentuados que causam a alguns pacientes considerável sofrimento físico e emocional. Uma vez que as larvas tenham completado o desenvolvimento ou tenham sido removidas, as lesões e o desconforto logo se resolvem. A invasão do olho ou de outros tecidos profundos pode apresentar grave morbidade e raramente é fatal para o paciente.
Apesar da destruição tecidual que podem causar, o local infestado frequentemente permanece livre de contaminação microbiana como resultado das secreções antibacterianas produzidas pelas larvas. Clínicos ocasionalmente introduzem larvas da “larva cirúrgica”, Lucilia sericata, intencionalmente como um meio de destruir tecidos não viáveis de feridas inoperantes.
Existem três elementos necessários para produzir uma infecção pós-operatória: um hospedeiro receptivo; contaminação por microorganismos e um meio de cultura de feridas para apoiar o crescimento bacteriano. O Centro de Controle e Prevenção de Doenças dos Estados Unidos informa que a taxa de infecção pós-operatória para uma cirurgia limpa e não contaminada é de <3%. A pele fornece uma grande barreira às bactérias invasoras, na medida em que uma vez estabelecido um portal de entrada, as bactérias podem penetrar nas camadas mais profundas onde a resistência é diminuída. A infecção em uma ferida fechada é muito mais problemática do que uma infecção superficial em uma ferida aberta. Durante o ambiente operatório, a contaminação da ferida pode ocorrer de várias fontes, incluindo punções de luvas, contaminação de coberturas estéreis e instrumentação, ou esfoliação ineficaz da pele. A duração do procedimento também pode ter um papel na contaminação da ferida, com a taxa de infecção quase dobrando a cada hora de operação. Portanto, não parece haver um fator único que influencie a contaminação da ferida. O estado fisiológico do paciente e da ferida antes e depois do procedimento cirúrgico parece ser um fator mais significativo no desenvolvimento de uma infecção pós-operatória do que a contaminação da ferida por bactérias.
Além da saúde geral do paciente e da contaminação da ferida, a ferida deve fornecer um meio de cultura para que as bactérias floresçam em uma infecção pós-operatória completa. Feridas isquêmicas ou necróticas fornecem um excelente meio de cultura para o crescimento bacteriano. Estes tecidos carecem de oxigênio e nutrientes suficientes para lidar com a cicatrização da ferida e a infecção iminente. A necrose pode ser devida à dessecação da ferida, eletrocauterização extensa, manuseio áspero do tecido, uso prolongado do torniquete, edema excessivo ou alta concentração de epinefrina. Corpos estranhos ou implantes também fornecem um bom meio de cultura para as bactérias. Suturas, próteses e dispositivos de fixação, todos diminuem localmente a resistência do hospedeiro às bactérias.

Como a gravidade da infecção da ferida aumenta, a resposta inflamatória aumentada tem um efeito negativo na cicatrização da ferida. As enzimas proteolíticas são liberadas das células inflamatórias, o que acelera a reabsorção das suturas enterradas, diminuindo o suporte da ferida e aumentando a deiscência da ferida. A partir da ferida aberta, amostras da drenagem podem ser coletadas para estudos de cultura e sensibilidade e coloração de Gram. Como a cultura pode levar alguns dias para retornar, antibióticos empíricos podem ser iniciados com base nos achados da coloração de Gram, a localização da infecção e os organismos mais prováveis encontrados naquela área. A primeira linha de cobertura é geralmente com um antibiótico que irá cobrir o Staphylococcus aureus até que as culturas laboratoriais estejam disponíveis, juntamente com a confirmação do organismo infectante e sensibilidade antibiótica.
Pode ser um desafio diferenciar o processo patológico precoce de uma infecção da resposta fisiológica normal de uma inflamação pós-operatória. Os sinais e sintomas da infecção precoce incluem dor grave não responsiva a analgésicos fortes, edema peri-incisional, eritema e calor radiante. Isto pode ser visto, entretanto, com formação de hematoma, gota aguda, inflamação, curativos apertados e gessos apertados. São os sinais e sintomas adicionais que se desenvolvem com infecção contínua que auxiliam no diagnóstico: febre, calafrios, suores noturnos, perda de apetite, estrias vermelhas e linfadenopatia. Estes sintomas geralmente se apresentam mais tarde no processo de infecção.
Os testes laboratoriais podem ajudar a confirmar a presença de infecção, bem como o(s) organismo(s) responsável(eis). A cultura e sensibilidade para determinar as bactérias e a cobertura antibiótica adequada é o padrão de cuidados para o manejo da infecção. Um hemograma completo com uma contagem elevada de neutrófilos e uma contagem elevada de leucócitos também apontará para uma infecção contínua. Entretanto, ele também pode ser elevado em resposta à própria cirurgia. As hemoculturas são raramente necessárias na cirurgia cutânea devido à raridade da bacteremia ou septicemia.
Uma variedade de bactérias pode ser cultivada a partir da ferida infectada no pós-operatório, sendo a mais comum a S. aureus. Isto é seguido de perto pela S. epidermidis, que antes era considerada como um contaminante da pele na cultura, mas agora está se tornando mais virulenta e é freqüentemente o organismo causador quando os implantes estão presentes. As infecções por Staphylococcus são eritematosas, inchadas e tenras com um abscesso localizado que consiste de pus cremoso grosso. Outra bactéria invasora comum é o grupo hemolítico A estreptococos (β). As infecções por estreptococos são intensamente vermelhas com celulite e calor extremo, mas não se observa purulência, apenas drenagem serosa ocasional. As infecções por estreptococos podem dissolver coágulos de fibrina e se espalhar rapidamente levando à septicemia se o diagnóstico for retardado. Bacilos Gram-negativos também podem ser isolados de uma infecção operatória, mas é mais raro em cirurgia cutânea do que os cocos Gram-positivos acima. Escherichia coli, Klebsiella, Proteus, Pseudomonas, Enterobacter e Serratia são as bactérias Gram-negativas mais comuns. Qualquer bactéria pode levar a uma infecção pós-operatória, mas com base no local da infecção e nas condições locais, alguns organismos, como as hastes Gram-negativas, Candida e bactérias anaeróbicas são muito menos comuns em cirurgia cutânea.

A melhor abordagem para a infecção pós-operatória é a prevenção. O cirurgião deve aderir ao protocolo estéril asséptico rigoroso perioperatório, bem como estar em alerta para quaisquer sinais e sintomas pós-operatórios que possam se correlacionar com um processo infeccioso insidioso. Os antibióticos profiláticos são universalmente aceitos como um método para diminuir a incidência de infecções pós-operatórias. Há alguma controvérsia e poucos dados científicos para fundamentar quando os antibióticos profiláticos são melhor utilizados e sob quais circunstâncias, mas existem diretrizes anedóticas aceitas que muitos cirurgiões seguem quando consideram o uso de antibióticos. Os antibióticos profiláticos são freqüentemente instituídos quando um procedimento envolve a implantação de um material estranho, como um enxerto de tecido, parafuso metálico ou implante, ou um procedimento cirúrgico que envolve dissecção extensa ou exposição prolongada de ferida de mais de 2 h.
Alguns hospitais agora estabeleceram protocolos antibióticos para os cirurgiões seguirem como parte de suas “Diretrizes de Melhores Práticas”. Um paciente comprometido por uma condição cardíaca ou defeito valvar, agentes imunossupressores ou doença vascular periférica também está em risco de uma infecção pós-operatória séria e potencialmente fatal, e frequentemente recebe um antibiótico profilático para tentar evitar estas complicações. A controvérsia em torno do uso de antibióticos profiláticos continua com relação a qual agente antibiótico selecionar e a duração apropriada da cobertura antibiótica. Alguns conceitos gerais são que o antibiótico deve estar nos tecidos antes da abertura e exposição da ferida, o antibiótico deve ser dirigido ao organismo causador mais provável e a duração do uso pode variar de uma única dose administrada no pré-operatório até um regime contínuo de até 24 h após a cirurgia. Além das 24 h, não parece haver maior proteção para o paciente. A escolha mais popular para antibiótico profilático é a cefazolina. A cefazolina é uma cefalosporina de primeira geração que é muito eficaz como antibiótico profilático devido aos níveis séricos relativamente altos, boa penetração óssea, longa duração, boa cobertura de Staphylococcus e alguma cobertura Gram-negativa, e custo razoável.
Se um paciente tem verdadeira penicilina ou alergia a cefalosporina, a clindamicina é uma boa alternativa com excelente cobertura contra Staphylococcus, excelente penetração tecidual e óssea, e é capaz de penetrar a glicocalyx bacteriana produzida em torno de implantes estranhos por S. epidermidis. A vancomicina tem sido muito popular no passado e freqüentemente utilizada em pacientes alérgicos à penicilina, entretanto, tem havido uma preocupação crescente com o desenvolvimento de cepas resistentes à vancomicina de S. aureus e S. epidermidis.
Com o diagnóstico de infecção surgindo no pós-operatório, o cirurgião deve excluir vários outros diagnósticos que possam se apresentar de forma semelhante, incluindo hematoma e resposta inflamatória grave. O paciente com infecção geralmente apresentará sinais constitucionais de infecção como febre, calafrios, suores noturnos, linfangite e linfadenopatia. Uma vez feito o diagnóstico clínico da infecção, o cirurgião deve agir rapidamente e com a finalidade de evitar complicações adicionais potencialmente mais graves. Radiografias são geralmente obtidas para uma linha de base para avaliar qualquer alteração óssea ou possível gás nos tecidos. Se houver drenagem, é obtida uma coloração de Gram e esta é seguida por uma cultura e sensibilidade.
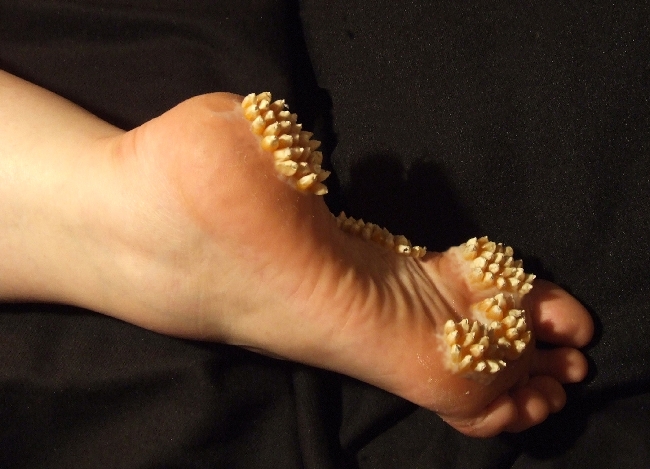
Antibióticos empíricos são frequentemente iniciados, mesmo antes do resultado da cultura estar disponível, para tentar intervir precocemente e diminuir a propagação da infecção. Se o paciente for levado ao centro cirúrgico, a cultura é repetida em condições estéreis e nos tecidos mais profundos para se obter uma identificação mais precisa do(s) organismo(s) envolvido(s) sem contaminantes cutâneos. Uma vez devidamente identificado o organismo, o antibiótico empírico pode ser substituído pelo antibiótico sistêmico terapêutico adequado com base nas sensibilidades e na ação bacteriocida do antibiótico com a menor toxicidade para o paciente. Este será geralmente um antibiótico parenteral, mas também pode ser aumentado com um antibiótico oral. Em algumas infecções, pode haver uma dúvida quanto à extensão da invasão bacteriana, caso em que uma ressonância magnética (RM) mostrará a extensão e a localização exata da formação de abscesso e alterações precoces da medula que podem indicar osteomielite. O tecnécio-99 também pode ser utilizado para avaliar a profundidade da infecção; entretanto, achados falso-positivos podem ser vistos tanto nas imagens de RM quanto nas de escaneamento ósseo, se o trabalho ósseo foi realizado intra-operatoriamente. Quase todas as infecções pós-operatórias requerem cobertura antibiótica, drenagem do pus da ferida e irrigação e desbridamento de qualquer tecido necrótico. Isto geralmente é realizado no ambiente operatório, mas também pode ser realizado à beira do leito.
A ferida é deixada aberta e pode ser fechada posteriormente através de fechamento primário retardado ou com permissão de cicatrização por intenção secundária. Nos estágios iniciais, muitas vezes é aconselhável embalar a ferida aberta com curativos estéreis ou gaze como iodophor. O cirurgião deve monitorar de perto o estado de mudança da ferida para ter certeza de que a infecção está reagindo adequadamente à intervenção. Se a infecção não parece estar respondendo, há muitas possibilidades: o organismo errado foi isolado; há outros organismos envolvidos não cobertos pelo antibiótico; o antibiótico não está sendo administrado em dosagem adequada ou não é capaz de penetrar no tecido infectado; uma cepa resistente de bactérias surgiu ou uma infecção profunda persistente ou abscesso está presente. O cirurgião deve avaliar estas possibilidades e alterar o plano de tratamento para resolver a infecção complicada. Um paciente necessitará de tranquilidade e apoio emocional durante o manejo desta virada de eventos.
Como a miíase causa danos consideráveis nos animais de criação, tenta-se controlar as moscas parasitárias onde a criação de ovinos, caprinos, vacas ou cavalos representa uma atividade econômica substancial. Atualmente é estabelecido um programa de controle na América Central, onde moscas machos de Cochliomyia hominivorax são esterilizadas e depois liberadas de forma controlada para competir com machos normais na fertilização de moscas fêmeas. É preciso ver se esta abordagem irá reduzir a incidência de miíase humana a longo prazo. Alguns tipos de miíase podem ser prevenidos se roupas, roupas de cama e toalhas não forem espalhadas no chão para secagem e se os tecidos forem engomados após a secagem.

